Estado de agregación de la materia: concepto, tipos y cambios de estado
Los estados de agregación de la materia nos ayudan a comprender cómo se comportan los materiales ante diferentes condiciones como la temperatura y la presión. Conocer estos estados y los procesos que los afectan es vital para entender una amplia gama de fenómenos físicos y químicos.
Tabla de contenidos
¿Qué son los estados de agregación de la materia?
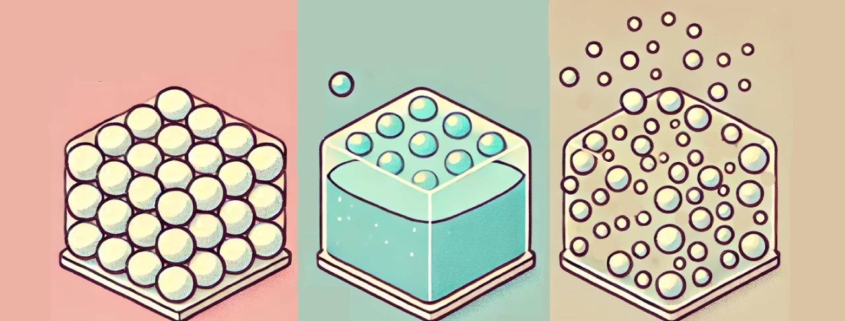
Los estados de agregación de la materia son las distintas formas en las que las partículas (átomos, moléculas o iones) que componen un material se organizan y se mueven. Los tres estados más comunes de la materia son: el sólido, el líquido y el gas.
Estado sólido
En este estado de agregación, las partículas están fuertemente unidas entre sí y ocupan posiciones fijas en una estructura bien definida, generalmente formando un cristal. Esto le da a los sólidos una forma y un volumen definidos. Las partículas en un sólido vibran en torno a sus posiciones fijas, pero no tienen libertad para moverse de un lugar a otro.
Estado líquido
En el estado líquido, las partículas están más separadas que en un sólido, lo que les permite moverse y deslizarse unas sobre otras. Aunque los líquidos tienen un volumen definido, no tienen una forma fija y adoptan la forma del recipiente que los contiene.
Estado gaseoso
Por el contrario, en el estado gaseoso las partículas están mucho más separadas entre sí y se mueven libremente y a gran velocidad. Los gases no tienen ni forma ni volumen definidos y tienden a expandirse para llenar todo el espacio disponible.
Cambios de estado de agregación
Los cambios de estado son las transformaciones físicas que ocurren cuando la materia pasa de un estado de agregación a otro. Estos cambios son procesos físicos porque no alteran la composición química de la sustancia, solo su disposición o el movimiento de sus partículas. Los principales cambios de estado son:
- Fusión: Es el proceso mediante el cual un sólido se convierte en líquido. Esto ocurre cuando la temperatura de una sustancia sólida se eleva lo suficiente como para que sus partículas adquieran la energía necesaria para superar las fuerzas que las mantienen en posiciones fijas.
- Solidificación: Es el cambio de un líquido a sólido. Al disminuir la temperatura, la energía cinética de las partículas disminuye, permitiendo que las fuerzas de atracción las fijen en posiciones más rígidas, formando un sólido.
- Vaporización: Es el proceso de cambio de un líquido a gas, que puede ocurrir de dos maneras: evaporación (que ocurre en la superficie del líquido a temperaturas inferiores al punto de ebullición) y ebullición (que ocurre en toda la masa del líquido a una temperatura específica).
- Condensación: Es el cambio de gas a líquido. Ocurre cuando un gas se enfría y sus partículas pierden suficiente energía cinética para acercarse y formar enlaces más fuertes, resultando en un líquido.
- Sublimación: Es el proceso en el cual un sólido se convierte directamente en gas sin pasar por el estado líquido. Este proceso requiere condiciones específicas de presión y temperatura, como ocurre con el hielo seco (dióxido de carbono sólido).
- Deposición: Es el proceso inverso a la sublimación, en el cual un gas se transforma directamente en sólido. Un ejemplo de esto es la formación de escarcha en las ventanas durante una noche fría.
Estos cambios de estado son fundamentales en la vida cotidiana y en la industria, ya que son la base de procesos como la refrigeración, la climatización y la fabricación de materiales.
¿Existen otros estados de la materia?
Además de los tres estados clásicos que hemos visto anteriormente (sólido, líquido y gas), existen otros estados menos comunes pero igualmente importantes que se producen bajo ciertas condiciones físicas y químicas, controladas o extremas.
- Plasma: Es un estado de la materia similar al gas pero con partículas cargadas eléctricamente, es decir, iones y electrones libres. El plasma se encuentra en condiciones de alta energía, como en las estrellas, incluido el Sol, o en fenómenos como las auroras boreales y los relámpagos. Este estado se forma cuando un gas se calienta a temperaturas extremadamente altas o se somete a un campo eléctrico fuerte.
- Condensado de Bose-Einstein: Es un estado de la materia que ocurre a temperaturas cercanas al cero absoluto (-273.15°C). En estas condiciones extremas, un grupo de átomos se comporta como si fuera una única entidad cuántica, lo que significa que todos los átomos ocupan el mismo estado cuántico. Este estado fue predicho por Albert Einstein y Satyendra Nath Bose en la década de 1920 y fue observado experimentalmente por primera vez en 1995.
- Condensado de Fermi: Similar al condensado de Bose-Einstein, pero ocurre con partículas que siguen la estadística de Fermi-Dirac (fermiones) en lugar de bosones. Este estado se produce en condiciones de baja temperatura y puede usarse para estudiar fenómenos como la superconductividad.
- Cristales Líquidos: Es un estado de la materia que tiene propiedades intermedias entre líquidos y sólidos. Los cristales líquidos fluyen como un líquido pero tienen una estructura ordenada similar a la de un sólido. Son ampliamente utilizados en pantallas de dispositivos electrónicos.
- Sólidos Amorfos: Aunque no son un estado diferente en sí mismos, los sólidos amorfos, como el vidrio, carecen de la estructura ordenada típica de los sólidos cristalinos, lo que les confiere propiedades únicas, como la transparencia.
Estos estados adicionales muestran la diversidad de formas en que la materia puede existir y cómo cambia bajo diferentes condiciones extremas de temperatura y presión. Son objeto de intensa investigación, especialmente en física y química cuántica, ya que pueden revelar nuevas propiedades de los materiales y contribuir al desarrollo de tecnologías avanzadas.